GABARITO E RESOLUÇÃO - CONCEITOS BÁSICOS
1-RESOLUÇÃO
As substâncias puras são formadas por moléculas quimicamente iguais.
A questão pede para dizer qual substância funde mais rápido (passa para o estado líquido). Analisando os gráficos, notamos que a temperatura de fusão da substância A é -116 ºC e da substância B é de – 89 ºC.
Concluímos que a substância A funde mais rápido, pois apresenta menor temperatura de fusão.
O processo utilizado para separar misturas homogêneas de líquidos com diferentes pontos de ebulição (líquido A 50 ºC e líquido B 118 ºC ... dados do gráfico) é a destilação fracionada.
2- RESP: C
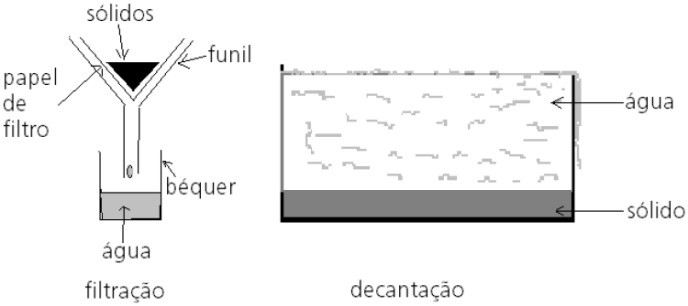
De acordo com o texto, a adição de substâncias químicas no tratamento da água, ocorre à formação de uma substância gelatinosa (flóculos) que aglutina as impurezas suspensas, facilitando a filtração (aspiração) para remover as impurezas.
Podemos concluir que o processo recebe o nome de floculação.
3- RESP: E
O texto informa que a vanilina é extraída a partir de vagens de orquídea espalhadas sobre bandejas, onde se utiliza o etanol (álcool etílico) como solvente.
Através deste processo ocorre a extração (dissolução) da vanilina.
4- RESP: C
Com o carbono, ocorre o fenômeno da alotropia, dando origem a substâncias puras simples e diferentes entre si. Para diferenciar um alótropo do outro, temos a atomicidade (número de átomos da substância simples) e a estrutura cristalina (maneira que os átomos estão agrupados).
Concluímos que a resposta correta é a C, onde temos diferentes estruturas cristalinas.
5- RESP: D
Misturas de líquidos homogêneos com diferentes PE são separados através da destilação fracionada.
Mistura sólida homogênea formada por naftalina e areia é separada por sublimação, pois a naftalina é um sólido que sofre sublimação.
Mistura sólida e líquida homogênea é separada por destilação simples.
A resposta correta é a C, onde encontramos os processos acima.
6- RESP: D
Quando o texto fala que o ouro é depositado sob o material sólido, está ocorrendo à separação de fases através da diferença de densidade.Para separar o ouro do mercúrio , a mistura é aquecida e o mercúrio com diferente temperatura deebulição é separado. Numa região próxima o mercúrio sofre a mudança de estado gasoso para o líquido, processo denominado de liquefação.
Nas alternativas, encontramos a resposta na alternativa D.
7- RESP: C
Com o carbono, ocorre o fenômeno da alotropia, dando origem a substâncias puras simples e diferentes entre si. Para diferenciar um alótropo do outro, temos a atomicidade ( número de átomos da substância simples ) e a estrutura cristalina ( maneira que os átomos estão agrupados ).
A única informação incorreta é a C, pois os isótopos pertencem ao mesmo elemento químico e não forma substâncias simples diferentes.
8- RESP: B
As misturas homogêneas são aquelas que apresentam um único aspecto.
- granito: quartzo + feldspato + mica – mistura heterogênea. ( trifásico )
- água mineral : contém sais dissolvidos – mistura homogênea.
-barra de ouro: metal nobre – substância pura simples.
-ar é uma mistura homogênea de gases – mistura homogênea.
-cloreto de sódio ( NaCl ) – substância pura composta.
DICA: • Pólvora negra: carvão + enxofre + salitre- sistema heterogêneo trifásico
Concluímos que a resposta correta é a B, pois encontramos duas misturas homogêneas.
9- RESP: B
Enquanto a garrafa está fechada, forma uma mistura homogênea, porque o gás está dissolvido no líquido. Após ser aberta, a pressão diminui e o sistema passa a ser heterogêneo, diminuindo a solubilidade do gás, logo passa a ser um sistema bifásico ( duas fases). O pH informado está entre 4,0 e 4,5 caracterizando uma solução ácida.
Cálculo do volume de álcool.
O texto informa que o teor de álcool é de 4,5% em volume. Isto significa que em cada 100 mL de cerveja temos 4,5 mL de álcool.
A alternativa correta é a B, pois ele admitiu um volume de 1 litro ( 1000 Ml ), onde teremos 45 mL de álcool.
100 mL cerveja ----------------- 4,5 mL de álcool.
1000 mL cerveja --------------- x x = 45 mL de álcool
10 - RESOLUÇÃO
a) Sem transferência de elétrons: reação de formação do hidróxido de Fe3+ ou do hidróxido de Cr3+.
Com transferência: reação entre o ferro metálico e o ácido, ou a reação entre o íon Cr6+ e o íon Fe2+.
b)