PROPRIEDADES COLIGATIVAS
(São as propriedades das soluções que dependem apenas do número de partículas dispersas e independem da natureza das partículas do soluto como tamanho, estrutura molecular ou massa).
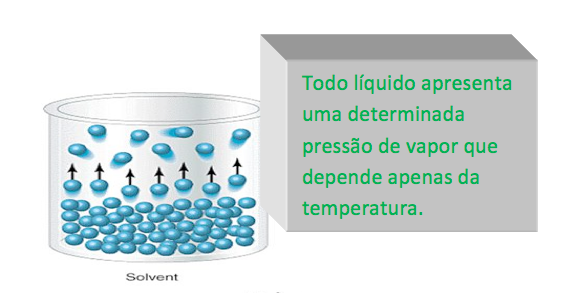
PRESSÃO MÁXIMA DE VAPOR
É a força exercida pelos vapores, em equilíbrio com a fase líquida em uma dada temperatura e pressão.
A pressão de vapor de um líquido está relacionada com a maior ou menor volatilidade.
A volatilidade depende do tipo de força intermolecular e da massa molecular de uma molécula. Dependendo da força intermolecular de uma molécula, o ponto de ebulição pode ser maior ou menor.Quanto maior a massa molecular , maior será o ponto de ebulição, portanto menor volatilidade e quanto maior for à força intermolecular maior será o ponto de ebulição porque quanto mais fortes forem às interações moleculares mais átomos da molécula estarão unidos, ou seja,será necessária maior quantidade de calor para romper essas ligações e assim o ponto de ebulição torna-se maior.
Ponto de fusão
É a temperatura no momento que uma substância no estado sólido começa a passar para o estado líquido.
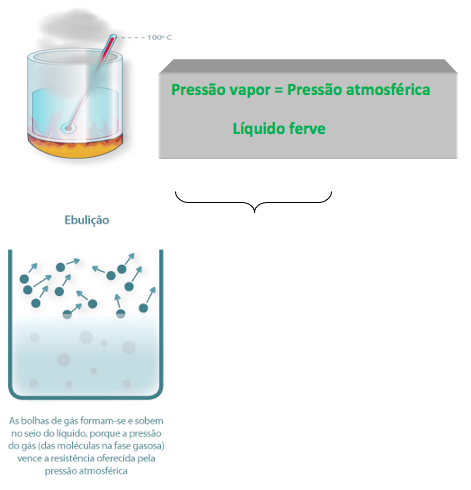
Ponto de ebulição:
É a temperatura no momento que um líquido começa a ferver.
Um líquido começa a ferver, quando a pressão de vapor deste líquido se igualar com a pressão atmosférica.
O ponto de fusão e de ebulição, sofre variação de acordo com a pressão atmosférica. Quanto maior a pressão atmosférica, maior será a temperatura de ebulição, ou seja, quanto maior a altitude, menor será a pressão e menor a temperatura de ebulição.
EFEITOS COLIGATIVOS.
Os efeitos coligativos dependem apenas do número de partículas do soluto iônico ou molecular, não volátil.
EFEITO TONOSCÓPICO (TONOMETRIA)
Quanto maior o número de partículas, menor será a pressão de vapor do líquido.
EFEITO EBULIOMÉTRICO (EBULIOMETRIA)
Quanto maior o número de partículas, maior será a temperatura de ebulição do líquido.
EFEITO CRIOSCÓPICO (CRIOMETRIA)
Quanto maior o número de partículas, menor será a temperatura de congelamento do líquido
DICAS PARA ENTENDER OS EFEITOS COLIGATIVOS.
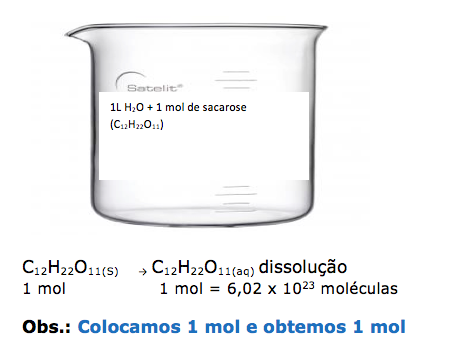
Soluto molecular
Soluto iônico
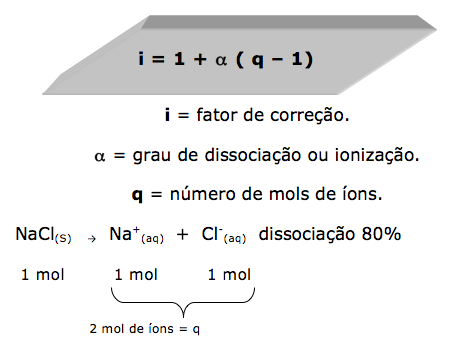
Nos compostos iônicos precisamos utilizar o fator de correção, denominado fator de Vant’Hoff (i).
Quando a dissociação for igual a 100%, o fator de correção será igual ao próprio número de mols de íons.
Quando a dissociação for diferente de 100%, utilizamos a fórmula a seguir, para determinar o valor de i.
Portanto:
i = 1 + α ( q – 1)
i = 1 + 0,8 ( 2 – 1 )
i = 1,8
PRESSÃO OSMÓTICA (π )
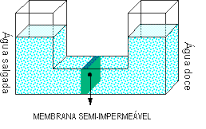
É a força exercida para impedir o processo de osmose.
Osmose: é passagem do solvente de uma solução diluída para uma solução concentrada, através de um membrana semipermeável.
A pressão osmótica é calculada pela fórmula:
p = ɱ.R.T.i
p = pressão osmótica.
ɱ = concentração molar.
R = constante universal dos gases.
T = temperatura em kelvin.
Portanto:
Compostos moleculares
p = ɱ.R.T
Compostos iônicos
p = ɱ.R.T.i
Solução isotônica: é aquela que apresenta pressão osmótica igual.
Solução hipertônica: possui pressão osmótica maior.
Solução hipotônica: possui menor pressão osmótica.
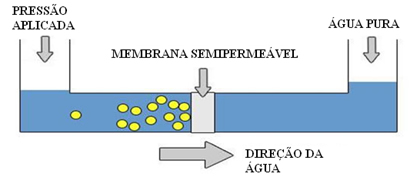
OSMOSE REVERSA
Na osmose reversa, o solvente da solução concentrada passa para uma solução diluída, através de uma membrana semipermeável.
Para ocorrer à osmose reversa, é utilizada uma pressão superior à pressão osmótica.
O processo de osmose reversa tem sido usado com o intuito de “potabilizar” a água por meio da dessalinização. Atualmente, a osmose reversa é considerada uma saída para o problema previsto da escassez de água.
Principais aplicações da osmose reversa na:
> indústria, é utilizada na fabricação de alguns tipos de bebidas, como certas águas minerais;
> agropecuária utiliza-se a osmose reversa na dessedentação de animais, na irrigação e hidroponia. Embora neste setor, ainda haja pouca difusão da técnica.
> dessalinização de águas salobras. Tem sido usado no nordeste do Brasil como solução para a problemática da seca nessa região;
> área da saúde, recebe destaque, principalmente, nos processos de hemodiálise;